「フォトバイオモジュレーション」ミトコンドリア代謝の活性化

Photobiomodulation for Alzheimer’s Disease: Has the Light Dawned?
Photonics. 2019 Sep;6(3):77. doi: 10.3390/photonics6030077
フォトバイオモジュレーション(Photobimodulation:PBM)

フォトバイオモジュレーション(PBM)とは、治癒を促進し、痛みや炎症を軽減し、組織の死滅を防ぐための赤色光または近赤外線(NIR)の治療的使用を指します。
以前は低レベルレーザー療法(LLLT)と呼ばれていましたが、発光ダイオード(LED)の普及によって、医療用レーザーと同等に機能するという報告もよく見られるようになりました。
レーザー以外の光源を用いたLLLTが増えてきたことから、Photobiomodulation therapy(PBMT)という用語を使用するようになりました。
PBM で有用であると想定されている発色団は、電磁スペクトルのさまざまな波長領域 (青、緑、赤、NIR)で吸収します。
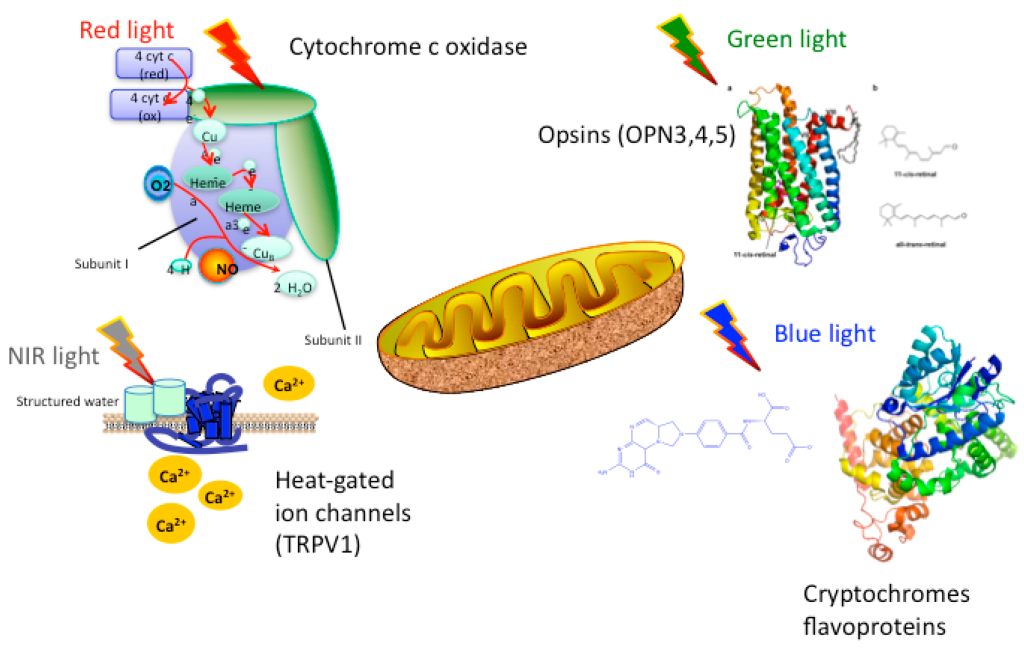
ミトコンドリアの電子伝達系は、一連の酸化還元反応を通じて、ミトコンドリアの内膜を通過する電子の移動を促進します。
これらの電子伝達ステップの最終的な結果は、ADP から高エネルギーの ATP を生成する ATP シンターゼ (Complex Ⅴ)の活性を駆動する、ミトコンドリア膜を横切るプロトン勾配を生成することです。
シトクロム C オキシダーゼ (CCO) は、ミトコンドリア外膜に位置する電子伝達鎖の末端酵素 (Complex Ⅳ)です。
CCO は、シトクロム C から分子状酸素への電子の移動を仲介します。
CCO は、13 の異なるポリペプチド サブユニットから構成される複雑なタンパク質であり、2種類の銅中心 CuA とCuB、2種類のヘム中心 heme-a と heme-a3 を含みます。
CCO は生物学的な光受容体であり、スペクトルの赤色および近赤外領域の光によって活性化されることがわかっています。
ミトコンドリアについては、関連記事をご参照ください ↓
ミトコンドリアの電子伝達系については、関連記事をご参照ください ↓
PBMによって、CCOの触媒中心における分子状酸素の還元のための電子の利用が増加し、ミトコンドリア膜電位(MMP)を増加させ、ATPの生成レベルを増加させます。
しかし、CCO が赤色および近赤外光の主要な発色団であることを支持する多くの証拠があるにもかかわらず、これがすべてではないことを示唆する報告も増えています。
ATPシンターゼ(Complex Ⅴ)の回転モーターの粘性摩擦を減少させて効率を高めて、ATP 生成の増加に反映されるとも考えられています。詳しくは関連記事をご参照ください ↓
水の分子吸収係数と細胞や組織における相対的な存在量を考慮すると、水が赤外波長 (>900 nm) で最も重要な発色団であることは明らかです。
それにもかかわらず、通常行われる PBM は、特に脳内の組織に過剰な加熱を引き起こしません。
実際、もし顕著な加熱効果があれば、頭皮の皮膚で感じられます。
PBM が 1064 nm もの波長で脳に強力な影響を与えることを説明する概念として、Pollack によって詳しく述べられた EZ水(構造水)の概念があります。
EZ水については、関連記事をご参照ください ↓
この EZ水 は、粘度や pH などのパラメーターに明確な物理的変化を引き起こす光放射を吸収します。
バルク水はEZ水と同程度にはIR光を吸収しないため、IR エネルギーがすべての水分子に吸収された場合に予想されるような、組織の検出可能なバルク加熱を引き起こしません。
熱エネルギーによるミトコンドリアのATPエネルギー生成については、関連記事をご参照ください ↓
メラニンによる光エネルギーから化学エネルギーへの変換については、関連記事をご参照ください ↓
アルツハイマー病

アルツハイマー病(AD)は最も一般的なタイプの認知症 (60% ~ 70%)であり、次に血管性認知症(25%)、レビー小体型認知症(15%)が続きます。
AD は、細胞外ベータアミロイド斑と、過剰リン酸化タウタンパク質によるニューロン内神経原線維変化を伴う、脳全体 (特に皮質)のびまん性萎縮を特徴とします。
しかし依然として、AD の正確なメカニズムは熱い議論の対象となっています。
Aβ ペプチド (40 または 42 アミノ酸)は、ベータおよびガンマ セクレターゼによるアミロイド前駆体タンパク質の連続的な酵素的切断によって形成されます。
Aβ 42 のレベルの増加は、アミロイド原線維の形成を引き起こし、最終的には老人斑に発展します。
これまでにアミロイド仮説が主流に研究されてた時期がありましたが、アミロイド斑は脳機能低下の原因ではなく、結果としての現象でマーカーであるという概念が生まれています。
アミロイド仮説については、関連記事をご参照ください ↓
またアミロイドの対立的な仮説は、タウに焦点を当てています。
タウタンパクは神経軸索内の微小管に結合しているタンパクで、 2 つのアイソフォーム (4R および 3R)があります。
ADの脳では、3R タウと 4R タウが過剰リン酸化状態で蓄積され、神経原線維変化を引き起こします。
微小管については、関連記事をご参照ください ↓
ADの大きな特徴として、神経炎症および反応性神経膠症(反応性グリオーシス)があります。
反応性グリオーシスについては、関連記事をご参照ください ↓
ADの脳内では、フリーラジカルを生成する鉄、アルミニウム、水銀などの特定の金属のレベルが増加していることから、酸化ストレスがアルツハイマー病の発症に関与していると考えられます。
活性酸素種(ROS)の発生と酸化ストレスについては、関連記事をご参照ください ↓
神経原線維変化およびアミロイド斑における過酸化脂質、4-ヒドロキシノネナール(4‐HNE)、タンパク質およびDNAへの酸化的損傷、終末糖化産物(AGEs)の増加などが起こります。
多価不飽和脂肪酸(PUFA)は、ROSによる酸化され過酸化脂質を生成した後、反応性の高い低分子のアルデヒド(4‐HNEなど)を生成します。詳しくは関連記事をご参照ください ↓
また、ROSによる酸化ストレスの根底には、還元ストレスが原因となっています。詳しくは関連記事をご参照ください ↓
脳におけるPBMのメカニズム
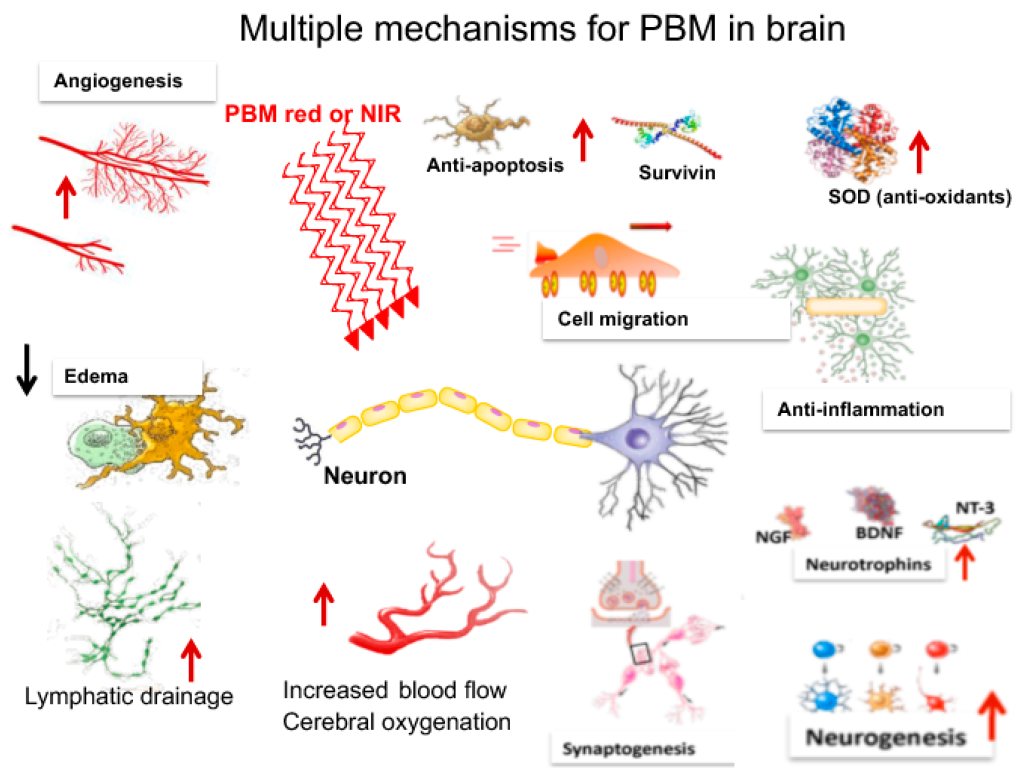
細胞内 ATP 産生の増加による代謝機能の改善が、PBMの最も強く支持されている作用機序の 1 つです。
一酸化窒素(NO)は、呼吸鎖における電子伝達を阻害します。
CCO は、特定の波長で光子エネルギーを吸収して NO を解離することにより、酵素活性を高めます。
これによって、ミトコンドリア膜電位 (MMP)が増加し、酸素消費量が増加して、ミトコンドリアによる ATP 生成が増加します。
さらに、PBMの結果として放出された NO は、血管を拡張し、脳血流を増加させ、脳への酸素供給を改善します。
PBM が神経保護、本質的に細胞を損傷から保護し、生存と寿命を促進し、アポトーシスシグナル伝達プロセスを逆転させる可能性があります。
正常な細胞では、CCOによる光の吸収により、ミトコンドリア膜電位(MMP)がベースラインを超えて増加し、ROS産生が短期間で急増します。
しかし、既存の酸化ストレス、興奮毒性、または電子輸送の阻害によりMMPが低下している細胞では、光吸収によりMMPが正常レベルに向かって増加し、ROS産生が減少します。
同様に、健康な細胞における PBM に対する典型的な反応は、細胞内 Ca 2+の短期間の増加です。
しかし、すでに過剰な Ca 2+を含む細胞(興奮毒性と呼ばれる現象)では、PBM は逆の反応を引き起こします。
つまり、過剰な細胞カルシウム レベルを低下させ、細胞の生存を促進し、酸化ストレスを低下させ、MMP を正常に戻します。
炎症は、細菌やウイルスなどの異物に対する自然免疫系の防御の 1 つです。
細胞レベルでは、転写因子 NF-κB が活性化されると発生します。急性炎症はプラスの影響を及ぼしますが、慢性炎症は非常にマイナスの影響を与える可能性があります。
神経変性疾患や気分障害を含む多くの病気は、少なくとも部分的には慢性炎症に起因していると考えられます。
炎症や慢性炎症については、関連記事をご参照ください ↓
PBM が炎症を鎮めるのに役立つ 1 つの方法は、シクロオキシゲナーゼ 2 (COX-2) 酵素の阻害によるものです。
低出力での635 nmの光照射が、細胞内ROSを減少させることによって、COX-2阻害を引き起こすことが明らかとなっています。
またPBM は、遊離 NF-κB の細胞レベルを調節することもできます。
ミクログリアは、プラーク、損傷したニューロンとシナプス、および感染因子を求めて中枢神経系を絶えず清掃しています。
マクロファージ系統の他の細胞と同様に、ミクログリアは多様な表現型をとることができ、組織の恒常性を維持するために機能をシフトする能力を保持しています。
マクロファージについては、関連記事をご参照ください ↓
M1 表現型は、エネルギー生産のための酸化的リン酸化から好気性解糖への移行を伴うことがわかっています。
PBM が、酸化的リン酸化に向けてミトコンドリア代謝を活性化できるため、ミクログリアの表現型を M1 から M2 に変化させる可能性があると考えられます。
まとめ

フォトバイオモジュレーション(PBM)とは、治癒を促進し、痛みや炎症を軽減し、組織の死滅を防ぐための赤色光または近赤外線(NIR)の治療的使用を指します。
シトクロム C オキシダーゼ (CCO) は、ミトコンドリア外膜に位置する電子伝達鎖の末端酵素 (Complex Ⅳ)です。
CCO は、特定の波長で光子エネルギーを吸収して NO を解離することにより、CCOの触媒中心における分子状酸素の還元のための電子の利用が増加し、酵素活性を高めます。
PBMの結果として放出された NO は、血管を拡張し、脳血流を増加させ、脳への酸素供給を改善します。
これによって、ミトコンドリア膜電位 (MMP)が増加し、酸素消費量が増加して、ATP 生成が増加します。
またEZ水(構造水) は、粘度や pH などのパラメーターに明確な物理的変化を引き起こす光放射を吸収します。
PBMによる血糖降下作用については、関連記事をご参照ください ↓





