脂肪酸代謝による活性酸素種(ROS)発生のリスク

私たちが日常生活や運動などで消費するエネルギー源は、主に糖質と脂質です。
一般的には、糖質(1gあたり4kcal)より脂質(1gあたり9kcal)の方が、効率がよいエネルギー源であると言われています。
しかし、私たちのエネルギー代謝には、プラスの面とマイナスの面があります。
その両面を考えた上で、エネルギー源について語るべきなのです。
活性酸素種(ROS)の発生と酸化ストレス

私たちは、ミトコンドリア内膜上の呼吸鎖複合体(電子伝達系Complex Ⅰ~Ⅳ)において、酸化還元反応を利用した電子伝達を行い、生体内で必要な90%以上のATPを産生しています。
Complex I ではNADH、Complex IIではコハク酸がそれぞれ酸化されて、ユビキノンを還元してユビキノールにします。
Complex IIIでユビキノールが酸化されて、シトクロムcを還元しています。複合体IVでシトクロムcが酸化されて、酸素分子(O2)に電子を伝達することで水(H2O)に還元します。
この過程で、ミトコンドリア内膜を隔ててH+勾配が生じて、膜電位が発生します。
それをComplex VであるF型H+-ATPase(F1F0)が、このH+勾配を駆動力としてATPを合成していきます。
ミトコンドリアの電子伝達系でのATP産生については、関連記事をご参照ください ↓
活性酸素種(reactive oxygen species:ROS)
活性酸素種(ROS)は、スーパーオキシド(O2•-)、過酸化水素(H2O2)、ヒドロキシラジカル(•OH)、一重項酸素(1O2)など、反応性が高い酸素種の総称です。
生体内のROSの主な発生源はミトコンドリアです。
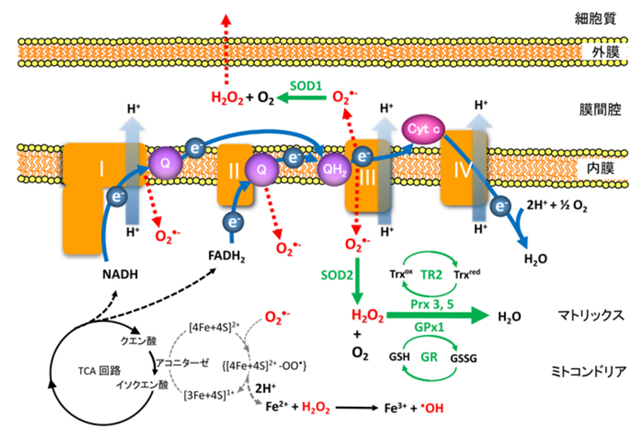
図は 東邦大学 より引用
ミトコンドリアの電子伝達系では、Complex IやComplex IIIから漏れ出した電子によって、酸素分子(O2)が一電子還元され、スーパーオキシド(O2•-)が発生します。
ミトコンドリアは、生体内の約95%の酸素を消費し、そのうち1~3%がROSを生成していると考えられています。
ミトコンドリアの膜間腔側に発生したスーパーオキシドはSOD1が、マトリックス側に発生したスーパーオキシドはSOD2が、酸素と過酸化水素(H2O2)に不均化し、過酸化水素はグルタチオンペルオキシダーゼやペルオキシレドキシンによって水へと還元されます。
生体内では、スーパーオキシドディスムターゼ(SOD)など抗酸化酵素により、ROSを消去する防御システムがあり、恒常性が維持されています。
しかし、ROSの過剰発生や抗酸化能が低下することによって、抗酸化防御システムが崩れた状態を「酸化ストレス」といいます。
ミトコンドリアについては、関連記事をご参照ください ↓
活性酸素と酸化ストレスについては、関連記事をご参照ください ↓
NADH 蓄積による「還元ストレス」が、活性酸素種(ROS)生成による「酸化ストレス」を引き起こします。詳しくは関連記事をご参照ください ↓
ミトコンドリア以外では、好中球やマクロファージなどの貪食細胞が、NADPAオキシダーゼの酵素によって、スーパーオキシドを生成して、体内の異物を取り込み分解除去しています。
呼吸基質によるATP産生量の違い

内呼吸に用いられるエネルギー源(有機物)は、主に糖質(グルコース)か脂質(脂肪酸)で呼吸基質と呼ばれています。
グルコースを呼吸基質とする場合と、脂肪酸を呼吸基質とする場合では、ミトコンドリアの電子伝達系に与える影響が、実は少し異なっています。
グルコースのエネルギー代謝
1分子のグルコースの好気性代謝では、解糖系・ピルビン酸→アセチルCoA変換・TCAサイクル(クエン酸回路)という一連の代謝過程で、4分子のATP、10分子のNADH、2分子のFADH2を生成します。
電子伝達系では、NADHからは10個のH+がマトリクスから膜間腔に移動、FADH2からは6個のH+がマトリクスから膜間腔に移動します。
F型H+-ATPase(F1F0)でATPを産生する場合には、4個のH+の濃度勾配による移動が必要となります。
つまり、1分子のNADHからは、2.5分子のATPが生成し、1分子のFADH2からは1.5分子のATPが生成することになります。
よって、1分子のグルコースからは、合計32分子のATPが生成することになります。
脂肪酸のエネルギー代謝
飽和脂肪酸のパルミチン酸(C15H31COOH)をエネルギー源とした場合について考えてみます。
パルミチン酸を活性化してパルミトイルCoAに変換するのに、ATPを消費します(最終的には2分子のATPを消費します)。
ミトコンドリアでβ酸化を7回行うことによって、8分子のアセチルCoA、7分子のNADH、7分子のFADH2を生成します。
1分子のアセチルCoAからTCAサイクルで、1分子のATP、3分子のNADH、1分子のFADH2が生成します。
1分子のパルミチン酸から、β酸化とTCAサイクルで、6分子のATP、31分子のNADH、15分子のFADH2が生成します。
電子伝達系からF型H+-ATPase(F1F0)によって、1分子のパルミチン酸から最終的には106分子のATPが生成することになります。
ココナッツオイルの主成分である中鎖脂肪酸のラウリン酸(C11H23COOH)の場合には、1分子のラウリン酸から最終的には78分子のATPが生成することになります。
以上のことより、グルコースより脂肪酸をエネルギー源とした方が、たくさんのATPを産生することができます。
これが糖質より脂質の方がエネルギー効率がよいと言われる理由です。
ATP(アデノシン三リン酸)・代謝については、関連記事をご参照ください ↓
呼吸脂質による活性酸素の発生量の違い

How to deal with oxygen radicals stemming from mitochondrial fatty acid oxidation
Philos Trans R Soc Lond B Biol Sci. 2014 Jul 5;369(1646):20130446. doi: 10.1098/rstb.2013.0446.
Bioessays. 2019 Jan;41(1):e1800180. doi: 10.1002/bies.201800180.
FADH 2 / NADH比とROS形成
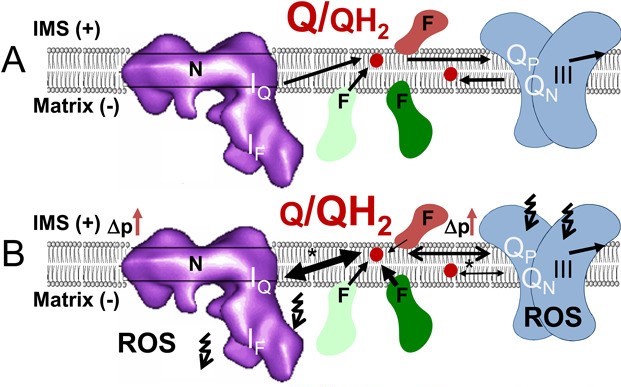
グルコースの代謝によって生成されるFADH2 / NADH比が0.2で、脂肪酸の代謝によって生成されるFADH2 / NADH比は、長鎖脂肪酸になるほど0.5に近づきます(パルミチン酸0.484、ラウリン酸0.478)。
ユビキノンはComplex ⅡのFADH2からの電子供与も受けるため、FADH2の比率が多くなると、Complex ⅠでのNADHからのユビキノンへの電子供与が競合によって低下します。
QH2/ Q比の増加によって、ユビキノンプールからの逆電子移動(RET)が起こって、Complex ⅠでROSの発生が増加します。
FADH2 / NADH比が高いと、活性酸素種(ROS)の生成が増加することがわかっています。
つまりグルコースのエネルギー代謝経路から脂肪酸のエネルギー代謝経路に切り替わると、活性酸素種(ROS)の発生が増加してしまい、酸化ストレスを引き起こすリスクが高まるということです。
長鎖脂肪酸のβ酸化は、ミトコンドリアだけでなくペルオキシソームでも行われることや、長鎖脂肪酸や酸化脂肪酸によって、UCP(脱共役タンパク質)の活性化が行われることは、ROSの発生を減らし酸化ストレスを回避するためと考えられています。
褐色脂肪細胞や脱共役タンパク質(UCP)については、関連記事をご参照ください ↓
ペルオキシソームのβ酸化

ペルオキシソーム
ペルオキシソームは1重の生体膜に包まれた細胞内小器官(オルガネラ)で、長鎖脂肪酸のβ酸化の代謝に関わっています。
私たちの細胞には、ミトコンドリアとペルオキシソームという2つの脂肪酸酸化に関わる小器官(オルガネラ)が存在します。
脂肪酸をβ酸化するという働きは共通していますが、その酸化反応が異なります。
ミトコンドリアでは、アシルCoAデヒドロゲナーゼによって、脱水素化(酸化反応)によって2重結合を導入してFADH2 を生成します。
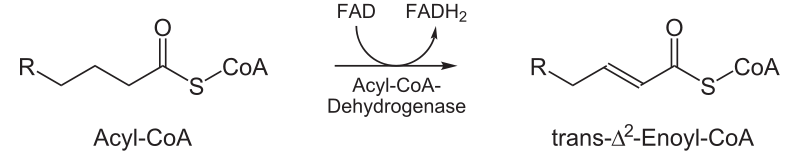
一方、ペルオキシソームでは、アシルCoAオキシダーゼによって、酸素(O2)との酸化反応によって2重結合を導入して、過酸化水素(H2O2)を生成します。
この反応がミトコンドリアとペルオキシソームのβ酸化の違いです。
ペルオキシソームでは、必ずROSである過酸化水素(H2O2)を生成します(FADH2を生成しません)
できた有害な過酸化水素は、ペルオキシソーム内にあるカタラーゼによって分解されます。
ミトコンドリアの場合、脂肪酸のβ酸化によって得られるアセチルCoA・FADH2・NADHは、TCAサイクルと電子伝達系と共役して、ATP産生に利用されます。
一方、ペルオキシソームにはそのようなATP産生機能がなく、脂肪酸のβ酸化によって生じるアセチルCoA・NADHは、直接ATP産生に利用されません。
ペルオキシソームは、ミトコンドリアと違って、ATP(エネルギー)産生とは共役していないのです。
ぺルオキシソームの脂肪酸のβ酸化は、生体内成分として利用できない脂肪酸を、脂肪酸リモデリング(必要な脂肪酸合成)を行う役割があります。
また、ミトコンドリア内でのROS発生を、軽減する役割があるのではないかと考えられます。
ペルオキシソームで特に長鎖脂肪酸のβ酸化を行うことにより、ミトコンドリアでのFADH2 / NADH比を下げています。
脂肪酸の種類や特性・脂肪酸リモデリングについては、関連記事をご参照ください ↓
まとめ

私たちは、ミトコンドリアの酸素を使ったエネルギー代謝により、大量のATPを獲得しています。しかし、それと同時に活性酸素種(ROS)による酸化ストレスのリスクを負っています。
私たちの細胞は、グルコースも脂肪酸もどちらも呼吸基質(エネルギー源)としてエネルギー代謝を行うことができます。
グルコースのエネルギー代謝の経路が流れている時には、脂肪酸のエネルギー代謝の経路が抑制され、脂肪酸のエネルギー代謝の経路が流れている時には、グルコースのエネルギー代謝の経路が抑制されています。
代謝酵素の働きが調整され、同時にグルコースと脂肪酸のエネルギー代謝を進めることができず、適宜切り替えを行っているのです。これはランドルサイクルと呼ばれています。
グルコースをエネルギー代謝する経路と、脂肪酸をエネルギー代謝する経路では、生成するFADH2 / NADH比が異なります。
それがミトコンドリアでの電子伝達系の複合タンパク質での、活性酸素種(ROS)の生成に影響を与えます。
脂肪酸のエネルギー代謝は、グルコースのエネルギー代謝と比較して、FADH2 / NADH比が高くなり、ミトコンドリアでの活性酸素種(ROS)の発生を増加させてしまいます。
肥満により脂肪酸のエネルギー代謝が活性化され、グルコースのエネルギー代謝が抑制されているのが、インスリン抵抗性の状態です。
高血糖による糖毒性(糖化リスク)だけでなく、脂肪酸のエネルギー代謝が中心になることで、ミトコンドリアでの活性酸素種(ROS)の発生を増加させ、酸化ストレスを引き起こすリスクが高まります。
酸化ストレスによって、ミトコンドリアの呼吸鎖(タンパク質)が障害を受けると、ミトコンドリア機能が障害されて、私たちにとって様々な負の影響がもたらされています。
ランドルサイクルについては、関連記事をご参照ください ↓
インスリン抵抗性の改善には、グルコースとフルクトースの相乗作用が有効です。詳しくは関連記事をご参照ください ↓





